小分子抑制剂显示出对抗YAP融合驱动的癌症的早期希望
辛辛那提儿童医院脑肿瘤中心的专家在研究一种罕见但致命的脑肿瘤时的一项意外发现也可能导致改善其他几种癌症的治疗方法,这些癌症都有一个共同的影响因素,称为YAP 融合蛋白。
该研究结果于 2023 年 2 月 2 日发表在Nature Cell Biology上,由共同第一作者胡晓华博士和吴晓平博士以及通讯作者、脑肿瘤中心科学主任Qing Richard Lu 博士领导。该作品还包括来自辛辛那提、克利夫兰、西雅图、中国上海和波兰华沙的 15 位合著者的贡献。
研究小组正在研究为什么在被诊断患有室管膜瘤 (EPN) 的儿童亚群中会发生致命后果,这是一种发生在大脑和脊柱的罕见癌症。每年约有 1,100 人被诊断患有 EPN,其中包括约 250 名儿童。
成年人通常会经历这些沿着脊髓发展的肿瘤,在许多情况下,它们可以通过手术切除。根据国家癌症研究所和临床肿瘤学会的数据,总体而言,此类癌症的五年生存率接近 84%。
然而,患有 EPN 的儿童更容易在大脑中形成肿瘤。虽然可以通过手术切除的肿瘤的存活率很高,但大约三分之一的 EPN 患儿尽管接受了手术、放疗和化疗,但仍会复发。对于这些孩子,复发几乎总是致命的。
EPN 肿瘤的确切原因尚不完全清楚。然而,患有 Turcot 综合征和 2 型神经纤维瘤病 (NF2) 等遗传病的儿童患这种癌症的风险增加。
关于 YAP 融合蛋白的新数据打开了大门
先前的研究已经表明,一组 EPN 肿瘤的生长在很大程度上是由 YAP 融合蛋白的形成驱动的。YAP1 基因本身会产生一种蛋白质,该蛋白质可阻断另一种名为 HIPPO 的基因的肿瘤抑制能力。但近年来,科学家们发现了一个完整的 YAP 蛋白家族,这些蛋白由 YAP1 与其他基因融合产生,以促进更具侵袭性的癌症肿瘤生长。已在皮肤癌、乳腺癌和各种称为肉瘤的软组织肿瘤的亚型中检测到 YAP 融合蛋白。
这项新研究表明,YAP 融合蛋白以不同于许多科学家认为的方式破坏人体的癌症防御能力。这些融合的 YAP 蛋白不是简单地增强 YAP1 活性,而是触发细胞核中“凝聚物”的形成,为驱动脑细胞转化和肿瘤形成提供平台。
通过研究这些平台的组成部分,该团队了解到可以通过阻断称为 BRD4 的基因表达调节剂的功能来防止它们形成肿瘤。这种蛋白质被称为转录因子,它发送关键信号以激活核凝聚物中的其他致癌基因。
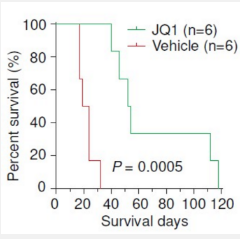
该团队在小鼠中测试他们的想法时取得了早期概念验证的成功,这些小鼠被诱导产生类似于人类 EPN 的肿瘤。用两种不同的 BRD4 抑制剂治疗的小鼠比未接受抑制剂的小鼠存活时间长得多。
这对患有 EPN 的人意味着什么?
可能需要几年的安全测试和相关工作才能启动临床试验,以衡量使用 BRD4 抑制剂治疗 EPN 患者的益处和风险。然而,到目前为止,在这种类型的癌症中存活下来的主要方法取决于成功的手术。传统形式的化疗对复发病例几乎没有益处。
“我们的研究结果表明,靶向生物分子凝聚物可能最终证明对治疗复发性 EPN 有益,”Lu 说。“但首先,需要更多的研究来建立这些发现。”
这对其他类型的癌症意味着什么?
通过建立一种成功的方法来减缓一种形式的 YAP 融合介导的癌症的生长,该研究表明类似的方法可能适用于其他类型。
“我们的研究表明,靶向相关分子过程可以降低 YAP 融合蛋白刺激肿瘤生长的能力,而不是试图阻止基因融合的发生,”Lu 说。
