脂质纳米粒子在基因治疗中非常有效
脂质纳米颗粒已被用于封装 CRISPR- Cas9并将其递送至小鼠细胞,在小鼠细胞中它在抑制靶蛋白表达方面非常有效。
基因疗法是治疗由基因突变引起的多种疾病的潜在模式。虽然它一直是一个多样化和深入研究的领域,但从历史上看,只有极少数患者接受过基因治疗——而且治愈的患者更少。2012 年,名为 CRISPR- Cas9的基因改造技术的出现彻底改变了基因疗法——以及整个生物学——它最近进入了治疗人类某些疾病的临床试验。
北海道大学的 Haruno Onuma、Yusuke Sato 和 Hideyoshi Harashima 开发了一种基于脂质纳米颗粒 (LNP)的新型 CRISPR- Cas9递送系统,可以大大提高体内基因治疗的效率。他们的发现发表在《受控释放杂志》上。
“基因疗法治疗疾病的方法大致有两种,”Sato 解释说,“离体,细胞在实验室中进行所需的修饰,然后引入患者体内,以及体内,对细胞进行治疗。患者改变他们体内的细胞。安全有效的体内治疗是基因治疗的最终目标,因为这对患者和医疗保健提供者来说都是一个简单的过程。LNP 可以作为安全有效地提供此类疗法的载体。”
CRISPR- Cas9由一个大分子组成,该大分子由Cas9蛋白和引导 RNA 组成。向导 RNA 与特定的互补 DNA 序列结合,Cas9蛋白切割该序列,使其能够被修饰。可以改变指导 RNA 以靶向要修饰的特定 DNA 序列。
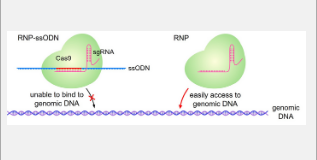
“在之前的一项研究中,我们发现额外的 DNA 分子,称为 ssODNs,确保 CRISPR- Cas9分子被加载到 LNPs (CRISPR-LNPs),”Harashima 解释道。“在这项研究中,我们再次使用了 ssODN,但它们经过精心设计,不会抑制向导 RNA 的功能。”
他们使用靶向转甲状腺素蛋白表达的指导 RNA,评估了 CRISPR-LNP 在小鼠模型中的有效性。具有在室温下从引导 RNA 解离的 ssODN 的 CRISPR-LNP 在降低血清转甲状腺素蛋白方面最有效:两次连续给药,间隔一天,将其降低 80%。
“我们已经展示了最佳的 ssODN 序列亲和力,可确保在目标位置加载和释放 CRISPR- Cas9 ;并且该系统可用于在体内编辑细胞,”Onuma 总结道。“我们将继续改进 ssODN 的设计,并开发最佳脂质配方以提高递送效率。”
