细胞如何管理其mRNA库存及其输出
在典型的细胞中,DNA编码的基因用于制造信使RNA(mRNA),而信使RNA又用于制造蛋白质,而基因表达的这一过程使细胞保持运转。每个细胞中的基因表达都受到调节,从而打开特定基因(制造蛋白质),并调高或调低它们的输出,从而驱动每个细胞的身份和行为。
然而,有一组不寻常的细胞,其中基因表达不能遵循其典型模式:发育中的卵子和它们可能生长的胚胎。在这些细胞中,在胚胎基因组准备好表达之前,有一个短暂的时期,此时基因不会产生新的mRNA。细胞必须使用的唯一遗传物质是先前由母体基因组制成的mRNA储备。
由于无法产生新的mRNA,细胞必须通过调整每个储存的mRNA在任何时间点产生的蛋白质数量来调节基因表达。他们还必须仔细安排去除母体mRNA的时间。如果细胞过早降解母体RNA,则没有可用的备份副本。如果它们降解母体RNA的时间太晚,可能会干扰胚胎基因组从母体基因组接管的交接。
由于这种独特的情况,发育中的卵子和胚胎已经进化出一种独特的系统来调节其mRNA。在3月8日发表在《发育细胞》杂志上的研究中,怀特海德研究所成员、麻省理工学院生物学教授、霍华德休斯医学研究所研究员DavidBartel以及他实验室的博士后KehuiXiang详细介绍了这些细胞的复杂调节系统用于管理其mRNA库存及其输出。
尾长决定RNA输出,但尾长由什么决定呢?
每个mRNA都有一个由一串腺苷或“A”组成的尾巴,腺苷是RNA的组成部分或碱基之一。这称为聚腺苷酸尾。研究人员知道,在发育中的卵子和早期胚胎中,mRNA的效率或用于制造蛋白质的速率取决于其尾巴的长度。尾巴越长,产生的蛋白质就越多。(在这个早期发育阶段之外,poly(A)尾起着不同的作用。)
由于尾部长度决定了mRNA的效率,Bartel和Xiang希望找出调节mRNA尾部长度的因素。任何调节尾长的因素最终都会调节这些细胞中的基因表达。
Xiang和Bartel通过观察每个mRNA中包含非编码或非翻译RNA的区域开始了他们的研究。每个mRNA都有非翻译区,这些区域可能包含不同的调控序列,影响其他分子与mRNA的相互作用。
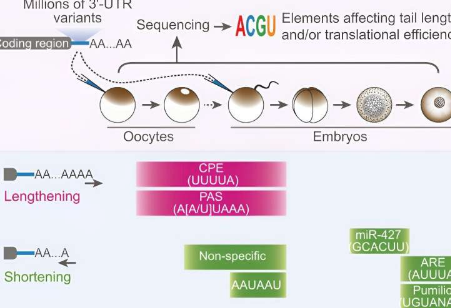
研究人员知道,mRNA的3'非翻译区包含两条序列,当RNA在细胞核外时,RNA尾部会被延长:一条序列称为细胞质多腺苷酸化元件(CPE),另一条序列称为多腺苷酸化信号(PAS)。
CPE和PAS都是结合位点,其序列与特定蛋白质相匹配。匹配的蛋白质结合到这两个位点,并与其他蛋白质一起形成导致尾部延长的机制。
研究人员知道PAS的序列,但CPE的正确身份一直难以捉摸。已经提出了各种序列,但许多经历尾部延长的mRNA不包含建议的CPE。
向和巴特尔使用系统方法来识别青蛙的CPE。他们创建了一个包含数百万个mRNA的文库,每个mRNA的3'非翻译区都有不同的序列。然后他们观察了青蛙发育中的卵中这些mRNA的尾部长度发生了什么变化。最终,这使他们能够缩小CPE的范围:UUUUA,五个碱基的序列。
他们发现的证据表明,这种CPE在进化中是保守的,并且是小鼠和人类共有的。他们还发现鱼胚胎的CPE略有不同,其中序列的最后一个碱基可以是A或U。
确定了CPE后,研究人员可以进行实验以确定是什么改变了CPE对尾长的影响。他们发现CPE两侧的碱基可以增强其效果——这可能解释了之前提出的一些CPE,它们往往是较长的序列。同样,最接近PAS的碱基可以改变其效果。
其他修饰因素包括mRNA中存在多少CPE和PAS拷贝、CPE与PAS的距离以及PAS与mRNA尾部的距离有多近。这些因素的结合决定了mRNA尾巴的长度,从而导致发育中的卵子和胚胎中的mRNA具有高度个性化的尾巴长度。
Bartel表示:“尾长变化非常复杂,通常发生在早期发育过程中,而这种变化是如何发生的一直是个谜。现在我们明白了为什么不同的mRNA表现如此不同。”说。
其他处于早期开发阶段的mRNA调节因子
Bartel和Xiang发现,虽然只有少数序列影响尾部延长,但在发育中的卵和早期胚胎中,多种序列都参与尾部缩短。不同的调节因子影响不同的mRNA,因此细胞可以在目标波中抑制母体mRNA。
许多mRNA的尾部在最初的大波中被缩短,然后较小的波以更个性化的方式缩短尾部,从而允许仔细协调脱离母体基因组控制的转变。
研究人员还确定了细胞抑制mRNA的方式,而与尾部长度无关。如果mRNA的3'非翻译区含有胞嘧啶或“C”碱基片段,则会抑制mRNA。此外,当未成熟的卵细胞在最终成熟之前处于休眠状态时,含有CPE的物质会抑制mRNA。
这一发现与之前的研究一致,并且考虑到Bartel和Xiang鉴定的许多含有CPE的基因与细胞分裂相关,这一发现也是有道理的。这些基因需要在休眠期间关闭,然后它们需要在卵子和胚胎发育过程中非常活跃。凭借其双重角色,CPE充当这些状态之间的优雅开关。
Xiang和Bartel的研究结果描绘了早期发育过程中mRNA复杂的调控系统。这使得精确调节成为可能,这样每个mRNA的输出都可以在每个发育阶段调节到正确的水平。这项工作揭示了单个受精卵细胞如何开始成为一个全新有机体的令人难以置信的过程。
后续工作可能会进一步阐明这些机制如何影响生育能力。Xiang和Bartel正在利用他们的发现创建可以预测给定mRNA尾部长度的算法。研究人员计划使用他们的预测工具来深入了解女性不孕症。例如,与延长mRNA尾部相关的基因序列突变如何影响卵子或胚胎的活力?
“由于3'非翻译区是非编码区,因此并未引起太多关注,但我们希望通过更多的基因组数据和改进的模型,我们可以查明可能具有潜在影响的人类遗传变异。“对生育能力的影响。这是我们动力的重要组成部分,”项说。
