铁有限环境中微生物作弊者的崛起研究揭示了它们的进化历史
竞争与合作是支配物种间进化和生态动态的基本力量。这些力量之间的平衡因生态环境而异,一些环境有利于促进互利的合作行为,而另一些环境则奖励最大化个体适应性的竞争策略。
在微生物群落中,分泌到环境中的化学物质提供了合作和利用的机会,在某些情况下会产生微生物“骗子”。这些作弊者利用其同行的合作行为,从分泌的化合物中受益,而无需支付生产的代谢成本。
在《分子生物学与进化》杂志上发表的一篇新文章中,威斯康星大学麦迪逊分校和范德比尔特大学的研究人员揭示了进化历史,为塑造铁限制微生物群落的合作和竞争动态提供了新的线索。
大多数生物体的许多生物过程都需要铁,但无法吸收环境中最常见形式的铁。因此,铁在生物群落中通常是有限的资源。为了克服这种稀缺性,微生物已经进化出利用铁载体从环境中清除铁的能力,铁载体是与环境中发现的铁类型具有高亲和力的分子。
铁载体在细胞内合成,然后分泌到环境中,与铁结合;然后,必须将与铁结合的分子输入回细胞,然后铁才能被释放并用于细胞代谢。分泌到环境中的铁载体可以被作弊者利用,他们通过吸收铁结合的铁载体而获得健康优势,而无需在其生产中投入能量。
虽然大多数酵母无法产生铁载体,但ChrisHittinger领导的研究小组发现Wickerhamiella/Starmerella(W/S)分支中的酵母可以产生一种称为肠杆菌素的铁载体。合成肠杆菌素所需的基因显然是从一种古老的细菌水平转移到W/S酵母的祖先中的。
然而有趣的是,一旦肠杆菌素铁载体与铁结合,W/S酵母就没有明显的方法重新导入它。“我们没有在细菌基因组中发现任何编码肠杆菌素转运蛋白的基因,”这篇新论文的主要作者孙亮说。
“对于酵母细胞来说,分泌肠杆菌素而不将其带回细胞进行铁吸收并不是明智之举,因此我们很好奇这些酵母如何可能利用与肠杆菌素结合的铁。”
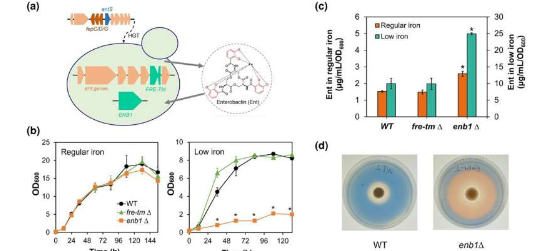
为了解决这个难题,研究小组搜索了Starmerellaombicola的基因组,寻找铁载体运输的替代机制。通过有针对性的基因破坏实验和系统基因组分析,研究小组确定了一个名为ENB1的基因对于圣博比科拉吸收肠杆菌素结合的铁至关重要。令人惊讶的是,ENB1是一种古老的真菌基因,其历史可能可以追溯到数亿年前,早于真菌谱系担子菌门和子囊菌门的分化。
进一步的分析揭示了酵母中ENB1的复杂历史。研究人员提出,ENB1是从W/S分支的祖先水平转移到酵母菌目的一个古老谱系的,该菌群包括酿酒酵母,用于制作面包、啤酒和葡萄酒。这种转移以及随后的基因复制和丢失,形成了目前在酵母中观察到的肠杆菌素利用的斑块分布。
这些发现对酵母铁吸收的历史有几个有趣的影响。由于肠杆菌素的吸收显然早于W/S酵母产生肠杆菌素的能力,因此该进化枝的祖先很可能是骗子,他们从环境中其他微生物产生肠杆菌素中受益。
随后,W/S进化枝从生态环境中的细菌获得了肠杆菌素生物合成基因,在该生态环境中,作为生产者比作为作弊者更有利。
根据对这些酵母分布的了解,该研究的作者提出,这种情况发生在昆虫肠道中,细菌、酵母和宿主之间对铁的竞争可能非常激烈。W/S酵母产生肠杆菌素并使用Enb1转运蛋白导入肠杆菌素的能力可能在这种竞争激烈、铁有限的环境中提供了适应性优势。
相比之下,ENB1在酿酒酵母等作弊者中的保留“可能与生态位有关,在生态位中,细菌和真菌共生者会产生肠杆菌素以应对铁缺乏,”该研究的作者说。“相反,ENB1的丢失可能发生在居住在铁可用性相对较高的环境中或缺乏肠杆菌素生产者的环境中的酵母中。”
虽然这些结果很有趣,但还需要更多的研究来充分揭示真菌和细菌肠杆菌素基因整合到W/S酵母中的机制。Sun表示,这些基因必须受到严格的共同调控,因为“肠杆菌素的分泌和输入不平衡可能会阻碍铁的吸收,从而导致酵母的生长缺陷。”
不幸的是,Sun指出,人们对这些酵母的代谢和调控网络还没有很好的了解,这可能会给未来的研究带来挑战,“因此,研究这一特定途径的调控可能需要额外的努力来填补其中的一些空白。”
尽管存在这些障碍,该系统为进一步研究酵母中铁载体转运蛋白的进化动力学及其在促进微生物群落内的合作和作弊中的作用提供了一个独特的模型。
